Apoptose
On appelle apoptose le processus par lequel des cellules déclenchent leur auto-destruction en réponse à un signal. C'est l'une des voies envisageables de la mort cellulaire, qui est physiologique, génétiquement programmée, indispensable à la...
Recherche sur Google Images :
Source image : imth.univ-lyon1.fr Cette image est un résultat de recherche de Google Image. Elle est peut-être réduite par rapport à l'originale et/ou protégée par des droits d'auteur. |
Définitions :
- Processus de mort programmée de la cellule qui a lieu naturellement comme étant une partie du développement, du maintien et du renouvellement normal d'un tissu. Il diffère de la nécrose, dans laquelle la mort cellulaire est génèrée par des facteurs externes (stress ou toxine). (source : biofondations.gc)
- Processus actif d'autodestruction par fragmentation de certaines cellules aboutissant à leur phagocytose. Note : Cette mort cellulaire, au contraire de la nécrose, n'est pas consécutive à une agression mais génétiquement programmée. (source : pages.infinit)
On appelle apoptose (ou mort cellulaire programmée, ou suicide cellulaire) le processus par lequel des cellules déclenchent leur auto-destruction en réponse à un signal. C'est l'une des voies envisageables de la mort cellulaire, qui est physiologique, génétiquement programmée, indispensable à la survie des organismes pluricellulaires. Elle est en équilibre constant avec la prolifération cellulaire. Au contraire de la nécrose, elle ne provoque pas d'inflammation : les membranes plasmiques ne sont pas détruites, du moins tout d'abord, et la cellule émet des signaux (en particulier, elle expose sur le feuillet externe de sa membrane plasmique de la phosphatidylsérine, un phospholipide normalement constitutif de son feuillet interne) qui permettront sa phagocytose par des globules blancs, surtout des macrophages.
Découverte et étymologie
L'apoptose (du grec : apo - au loin et ptosis - chute) a été mise en évidence en 1972 par John Kerr, Andrew Wyllie et Alastair Curie lors de l'étude de tissu par microscopie électronique[1].
Ils choisirent le mot «apoptose» (apoptosis) pour décrire le phénomène de mort cellulaire naturelle. Ce mot provient d'une locution grecque évoquant la «chute des feuilles»[2]. Elle avait déjà été employée en médecine par Hippocrate de Kos (460-377 av. J. C. ) dans son traité De Instruments de réduction pour décrire la décomposition des tissus après la mort («chute des os») [2], [3].
Exemples de rôles physiologiques
Morphogenèse
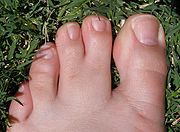
Par exemple la naissance des doigts. Au début de sa formation, la main est comparable à une moufle (ou une palme), puis les cellules se trouvant entre les futurs doigts disparaissent.
De même, la disparition de l'appendice caudal, chez le fœtus humain, est due à ce phénomène d'apoptose.
Elle joue un rôle dans la formation du cerveau : particulièrement tôt dans l'embryogenèse, le cerveau subit une vague apoptotique qui le remodèle. Par la suite, les neurones forment entre eux des liaisons synaptiques au hasard, et une deuxième vague apoptotique élimine ceux qui n'ont pas établi de liaisons utiles.
Elle peut aussi avoir un rôle moteur, la rétraction des cellules mortes entraînant la mobilisation des tissus voisins. Ce mécanisme a surtout été décrit chez l'embryon de la drosophile[4].
Dispositif immunitaire
En réponse à la naissance d'un antigène étranger dans le corps, des lymphocytes B se mettent à produire chacun un anticorps spécifique, en recombinant au hasard leurs gènes d'immunoglobulines (recombinaison VDJ). Ceux qui produisent des anticorps inactifs ou autoimmuns sont éliminés par apoptose. En cas d'infection virale, les lymphocytes T cytotoxiques produisent des molécules toxiques pour les cellules infectées; ils sont détruits par apoptose quand l'infection est maîtrisée. C'est le cas dans l'infection par le VIH mais cette voie entraîne ensuite des effets néfastes car les LT4 détruits en grande quantité ne peuvent plus sécréter les interleukines à l'origine de la sélection et de l'augmentcation clonale.
Différenciation intestinale
Les cellules intestinales sont en perpétuel renouvellement (avec une durée de vie de quelques jours uniquement) et migrent du bas des cryptes vers le sommet des villosités intestinales de l'intestin grêle où elles assurent leur fonction d'absorption des nutriments. Ultimement elles se décrochent et enclenchent un phénomène apoptotique spécifique nommé anoikis , dû à la perte de contact cellule-cellule ou cellule-matrice extracellulaire.
Dédifférenciation mammaire
Les acini des glandes mammaires après la période d'allaitement, et en absence du maintien du signal de prolifération/différenciation dû à la prolactine, vont se résorber, et perdre un nombre important de cellules épithéliales par un processus d'apoptose.
Causes
Une cellule normale a constamment besoin que le corps lui confirme son utilité, aux moyens de facteurs de croissance. La perte de ces signaux peut déclencher un processus apoptotique.
Des signaux émis à la suite des dommages subis par l'ADN (par exemple suite à une irradiation aux rayons UV ou aux rayons X) sont capables de déclencher l'apoptose : en effet c'est alors soit une cellule potentiellement cancéreuse, soit une cellule complètement dysfonctionnelle. Dans les deux cas, cette cellule doit être éliminée sans dommage pour le reste du tissu adjacent.
Des signaux hormonaux, surtout par les glucocorticoïdes, peuvent déclencher l'apoptose. C'est un mécanisme important de régulation du dispositif immunitaire.
Stress du réticulum endoplasmique : quand une cellule a un problème dans la conformation d'une protéine, qui aboutit à une accumulation de cette protéine dans le réticulum endoplasmique, elle peut entrer en apoptose.
La perte des contacts entre certaines cellules, ou bien entre ces cellules et leur matrice extracellulaire environnante induit de façon extrêmement rapide un processus apoptotique nommé anoikis .
L'apoptose peut aussi être causée par la dégradation des télomères des chromosomes. Elle peut être inhibée par les télomérases. Ce processus est aussi nommé horloge biologique.
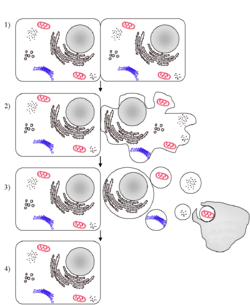
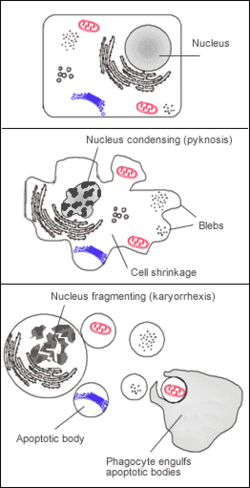
Manifestation cytologique
L'apoptose se manifeste sur ces cellules isolées (non regroupées). On constaste sur les cellules concernées une compaction et une marginalisation de la chromatine nucléaire ainsi qu'une convolution des membranes cytoplasmiques et nucléaires et une condensation du cytoplasme.
L'intégrité des membranes est conservée au cours du processus apoptotique évitant ainsi toute réaction inflammatoire. Les corps apoptotiques sont protégés par une enveloppe membranaire issue de la convolution des membranes..
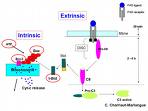
Mécanisme intracellulaire
Le mécanisme d'apoptose est gouverné par deux voies principales d'activation :
- une voie dite extrinsèque, impliquant des récepteurs appartenant à la superfamille des récepteurs au TNF,
- une voie dite intrinsèque mettant spécifiquement en jeu la mitochondrie ; cette voie est gouvernée par des protéines appartenant à la superfamille de Bcl-2.
Ces deux voies amènent à l'activation de protéases à cystéine nommées caspases, responsables des phénomènes morphologiques et biochimiques observés : exposition de phosphatidylsérine à la surface de la membrane cellulaire, arrêt de la réplication, fragmentation du noyau et du cytosquelette entraînant la formation de corps apoptotiques phagocytés par les cellules environnantes.
Voie extrinsèque
Dans l'état des connaissances actuelles, il semble que le mécanisme d'activation du récepteur Fas puisse être étendu aux autres récepteurs de mort. La signalisation par Fas recrute un complexe composé d'une molécule adaptatrice FADD (Fas Associated Death Domain) et de la procaspase-8. FADD se lie à travers son propre domaine de mort à ceux des récepteurs Fas. FADD contient aussi un domaine qui se lie à la procaspase-8. La formation de ce complexe entraîne le clivage de la caspase-8 qui est alors produite sous sa forme dimérique active, puis la cascade d'activation séquentielle des différentes caspases parmi lesquelles la caspase-3. Ces différentes protéases effectuent le clivage de plusieurs molécules, parmi lesquelles des protéines de structure et des protéines impliquées dans les dispositifs de réparation cellulaire. Il existe 2 voies de transduction du signal de la voie Fas, dépendant du type cellulaire. Dans les cellules de type 1 comme les thymocytes, la caspase 8 active directement la caspase 3. Dans les cellules de type 2 comme les hépatocytes, la caspase 8 active Bid, provoquant la libération du cytochrome c. L'association cytochrome c/APAF1 active la caspase 9 qui active à son tour la caspase 3.
Voie intrinsèque
La grande famille des protéines homologues à Bcl-2 joue un rôle majeur dans la régulation de l'apoptose. Cette régulation passe par la modulation de l'activité de certaines caspases, essentiellement la caspase 9. Ainsi, en empêchant la libération du cytochrome c par la mitochondrie, Bcl-2 et Bcl-XL inhibent la formation du complexe APAF1/cytochrome c/caspase 9 indispensable à l'apoptose. La mitochondrie joue un rôle clé dans la régulation de l'apoptose. En effet, la phase effectrice de l'apoptose comporte l'ouverture des pores de transition de perméabilité des mitochondries. Ces pores sont des canaux oligo-protéiques constitués au niveau de la membrane externe par la porine (ou VDAC : Voltage Dependent Anion Channel), sur la membrane interne par l'ANT (Adenine Nucléotide Translocator). Suite à l'ouverture de ces pores, il y a libération de molécules pro-apoptotiques telles que le cytochrome c, les caspases 2, 3 et 9 mais aussi l'Apoptosis Inducing Factor (AIF). L'AIF est une des molécules pro-apoptotiques libérées de la mitochondrie, il est situé dans l'espace intermembranaire mitochondrial. C'est une molécule possédant une double fonction :
Fragmentation de l'ADN
Durant l'apoptose, l'ADN est digéré de façon particulièrement spécifique en fragments dont les tailles sont des multiples de 180 paires de bases, ce qui cause une distribution particulièrement caractéristique des fragments d'ADN en «échelle» quand qu'ils sont scindés par électrophorèse suivant leur taille. Cette taille est révélatrice de l'espacement entre deux nucléosomes consécutifs. Cette digestion est assurée par les protéines CAD (Caspase Activated DNase), existant en temps normal sous forme inactive en association avec une ICAD (Inhibitor of Caspase Activated DNase). Cette ICAD cache la séquence NLS de CAD et le clivage de cette association par une caspase va permettre à la protéine CAD de rentrer dans le noyau, qui jouera son rôle de DNase clivant l'ADN.
L'un des mécanismes de l'apoptose dans les cellules cardiaques post ischémiques semble consister en la nitration des protéines cellulaires par un excès de peroxynitrites [1]. Ces peroxynitrites induisent aussi l'apoptose des monocytes [2] et des lymphocytes T [3]
Par exemple lorsque les cellules ne reçoivent pas en permanence de leurs voisines des messages inhibant leur autodestruction, elles disparaissent spontanément.
Maladies ou affections induites par le blocage de l'apoptose
Les cellules cancéreuses sont le plus souvent des cellules dans lesquels ce mécanisme ne fonctionne plus. Elles survivent et se multiplient en dépit d'anomalies génétiques survenues au cours de la vie de la cellule, tandis que normalement elles auraient dû être détruites par apoptose.
La réactivation du mécanisme d'apoptose a pu cependant être obtenu chez des cellules cancéreuses de rat[5].
Certains pathogènes empêchent l'induction de l'apoptose, comme par exemple HHV8 (herpesvirus responsable du sarcome de Kaposi), code la protéine v-FLIP empêchant l'apoptose induite par les récepteurs de mort.
Certaines maladies neurodégénératives comme les tauopathies, sont aussi des maladies où les mécanismes apoptotiques sont impliqués, conduisant à la survivance de protéine tau pathogène qui peut alors s'accumuler anormalement, jusqu'à la mort de la cellule nerveuse. C'est le cas de la paralysie supranucléaire progressive, de la maladie d'Alzheimer, etc.
Maladies ou affections causées par l'activation intempestive de l'apoptose
Des recherches récentes semblent montrer que le développement du sida comme maladie serait lié au déclenchement intempestif de l'apoptose des lymphocytes gérant la réponse immunitaire, ce qui permet le développement de maladies et infections opportunes. Cela ne remet pas en cause le rôle actif du virus VIH comme cause effective de cette maladie, quoique ce dernier soit bien détecté et tué par les lymphocytes.
Cependant le blocage du virus par les anticorps produits par les lymphocytes conduirait le virus à produire avant sa destruction complète une réponse chimique de défense conçue pour provoquer l'apoptose massive de l'ensemble des lymphocytes voisins, ou alors à faire fabriquer par les macrophages (qui absorberaient le virus neutralisé par les anticorps en même temps que le message chimique provoquant leur apoptose) cette réponse chimique qui provoquerait «à distance» le suicide de nombreux autres lymphocytes voisins alors même qu'ils n'ont jamais été directement en contact avec le VIH. En d'autres termes, le VIH provoquerait une réponse exacerbée du dispositif immunitaire contre lui-même. C'est alors un effet «boule de neige», où un dispositif morphologique est détourné de ses fonctions par une réponse non contrôlée, comparable à d'autres phénomènes auto-induits comme les allergies (elles aussi liées à un facteur déclenchant externe).
En provoquant cette réaction, une partie des copies du VIH parviendrait ainsi à échapper à l'action des lymphocytes T, dont un grand nombre se sont apoptosés après que quelques-uns d'entre eux uniquement ont neutralisé de nombreux virus voisins. Cela expliquerait aussi pourquoi l'éradication totale du virus par le dispositif immunitaire n'est pas envisageable sans une aide extérieure non sensible au phénomène de l'apoptose (une aide apportée par les médicaments anti-rétroviraux qui s'attaquent particulièrement au VIH pour éviter que les lymphocytes s'en chargent en activant alors l'apoptose de leurs voisins par l'action ultérieure des macrophages éliminateurs).
La compréhension des mécanismes chimiques de l'apoptose pourrait ainsi pallier cette fragilité intrinsèque du dispositif immunitaire, et permettre par conséquent le développement d'un type de vaccin spécifique, non conçu pour activer la réponse immunitaire contre le VIH (puisque celle-ci a bien lieu naturellement et produit de nombreux anticorps) mais à bloquer le déclenchement intempestif de l'apoptose des lymphocytes T CD4 chargés de leur neutralisation (et de la neutralisation des autres sources d'infection). Dans le cas du sida, on ne sait pas précisément quel lymphocyte possède cette fragilité (dangereuse seulement pour les autres types de cellules mais pas lui-même directement), mais on peut penser qu'elle se situe au niveau des macrophages chargés d'éliminer les virus neutralisés par les anticorps.
Ce comportement intempestif des mêmes macrophages (les poubelles de l'organisme qui peuvent générer par leur action des tas de produits toxiques et agents chimiques complexes à éliminer isolément) est aussi impliqué dans d'autres types de réactions exacerbées de l'organisme comme certaines allergies (où cette réaction, particulièrement beaucoup auto-entretenue, se fait à destination d'autres types de cellules que les lymphocytes immunitaires), et est soupçonné aussi dans d'autres types de maladies dégénératives (qui possèdent aussi un facteur déclenchant externe, pas obligatoirement de nature infectieuse) ou certaines réactions exacerbées face à un stress (par exemple l'extension des brûlures).
Bibliographie
- Jean-Claude Ameisen, La Sculpture du vivant : Le suicide cellulaire ou la mort créatrice, Point Seuil, 2003.
Voir aussi
Liens externes
- Les mécanismes moléculaires de l'apoptose - J. -E. RICCI
- Cell Death & Differentiation : la revue scientifique mondiale sur l'apoptose.
- Cours sur l'apoptose et autres processus cellulaires de la faculté de Médecine d'Angers
Notes
- ↑ Kerr JFR, Willie AH, Currie AR. Apoptosis : a basic biological phenomenon with wide-ranging implications in tissue kinetics. Br J Cancer 1972 ; 26 : 239-57. PMID :4561027
- chap 2, l'apoptose de la thèse de Doctorat en sciences vétérinaires, Identification de nouveaux mécanismes régulateurs de l'apoptose des granulocytes, 2007.
- ↑ Hellenic journal of nuclear medicine, The Journal of the Hellenic Society of Nuclear Medicine, Hell J Nucl Med 2008, 11 (1) : 2-4. Useful known and unknown views of the father of modern medicine, Hippocrates and his teacher Democritus
- ↑ Davidson LA, Apoptosis turbocharges epithelial morphogenesis, Science, 2008 :21;1641-1642
- ↑ Athanasiou A, Smith PA, Vakilpour S, et al (2007). Vanilloid receptor agonists and antagonists are mitochondrial inhibitors : how vanilloids cause non-vanilloid receptor mediated cell death. Biochem. Biophys. Res. Commun. 354 (1) : 50–5. doi :10.1016/j. bbrc. 2006.12.179. PMID 17214968.
- ↑ Kerr JFR, Willie AH, Currie AR. Apoptosis : a basic biological phenomenon with wide-ranging implications in tissue kinetics. Br J Cancer 1972 ; 26 : 239-57. PMID :4561027
- chap 2, l'apoptose de la thèse de Doctorat en sciences vétérinaires, Identification de nouveaux mécanismes régulateurs de l'apoptose des granulocytes, 2007.
- ↑ Hellenic journal of nuclear medicine, The Journal of the Hellenic Society of Nuclear Medicine, Hell J Nucl Med 2008, 11 (1) : 2-4. Useful known and unknown views of the father of modern medicine, Hippocrates and his teacher Democritus
- ↑ Davidson LA, Apoptosis turbocharges epithelial morphogenesis, Science, 2008 :21;1641-1642
- ↑ Athanasiou A, Smith PA, Vakilpour S, et al (2007). Vanilloid receptor agonists and antagonists are mitochondrial inhibitors : how vanilloids cause non-vanilloid receptor mediated cell death. Biochem. Biophys. Res. Commun. 354 (1) : 50–5. doi :10.1016/j. bbrc. 2006.12.179. PMID 17214968.
Recherche sur Amazone (livres) : |
Voir la liste des contributeurs.
La version présentée ici à été extraite depuis cette source le 06/11/2009.
Ce texte est disponible sous les termes de la licence de documentation libre GNU (GFDL).
La liste des définitions proposées en tête de page est une sélection parmi les résultats obtenus à l'aide de la commande "define:" de Google.
Cette page fait partie du projet Wikibis.


 Accueil
Accueil Recherche
Recherche Début page
Début page Contact
Contact Imprimer
Imprimer Accessibilité
Accessibilité