Chaîne respiratoire
La chaîne respiratoire est constituée d'un ensemble complexe de protéines membranaires de la mitochondrie des cellules eucaryotes qui servent à réoxyder les cœnzymes NADH et ubiquinone qui ont été réduits surtout au cours du cycle de Krebs.
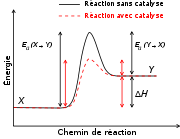
La chaîne respiratoire est constituée d'un ensemble complexe de protéines membranaires de la mitochondrie des cellules eucaryotes qui servent à réoxyder les cœnzymes NADH et ubiquinone (CoQ) qui ont été réduits surtout au cours du cycle de Krebs. Cette réoxydation s'accompagne de la création d'un gradient transmembranaire de protons. Ce gradient est une forme de stockage de l'énergie contenue dans les cœnzymes, qui dérive elle-même de l'énergie contenue dans les molécules dégradées au cours du catabolisme. Le gradient de proton va servir à fabriquer de l'ATP, molécule énergétique universellement utilisable, au niveau de l'ATP synthase, une protéine membranaire mitochondriale. Ce mécanisme de phosphorylation oxydative a été découvert par Peter Mitchell, ce qui lui a valu le prix Nobel de chimie en 1978[1]. Ce mécanisme est aussi connu sous le nom de Théorie chimiosmotique (de Mitchell). Additionné à la synthèse d'ATP par les ATP synthase on l'appelle phosphorylation oxydative.
Origine des réactifs de la chaîne respiratoire
Lors des réactions du catabolisme que sont la glycolyse (dans le cytosol) et le cycle de Krebs (dans la mitochondrie) il y a production de
Enchaînement des dispositifs d'oxydoréduction de la chaîne respiratoire
- Remarque
- L'enchaînement indiqué ici concerne les organismes eucaryotes, la chaîne respiratoire au niveau de la mitochondrie.
L'ordre dans lequel on trouve les éléments de la chaîne respiratoire (figure 1) dépend de leur potentiel standard d'oxydoréduction (tableau 1).
| Dispositifs rédox | Potentiel standard (à pH = 7 et 25 °C) |
|---|---|
| NAD+/NADH | -0, 32 V |
| FP/FPH2 | -0, 14 V |
| CoQ/CoQH2 | -0, 09 V |
| Cytb Fe3+/Cytb Fe2+ | +0, 04 V |
| CytC1 Fe3+/CytC1 Fe2+ | +0, 22 V |
| CytC Fe3+/CytC Fe2+ | +0, 26 V |
| Cyt (a+a3) Fe3+/Cyt (a+a3) Fe2+ | +0, 29 V |
| ½O2/O2- | +0, 82 V |
La réaction de synthèse d'ATP : 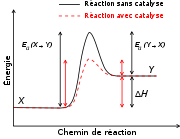
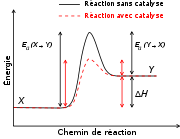
Est une réaction endergonique, elle a besoin d'énergie pour avoir lieu. Sa variation d'enthalpie libre standard (ΔG°) est égale à + 30 kJ/mol.
Lors de la chaîne respiratoire, trois réactions libèrent suffisamment d'énergie (variation d'enthalpie libre standard (ΔG°) est inférieure ou égale à - 30 kJ/mol) :
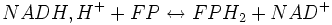 ΔG° = - 42 460 J. mol−1 ;
ΔG° = - 42 460 J. mol−1 ;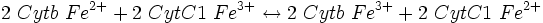 ΔG° = - 34 740 J. mol−1 ;
ΔG° = - 34 740 J. mol−1 ;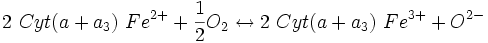 ΔG° = - 102 290 J. mol−1 ;
ΔG° = - 102 290 J. mol−1 ;
Inhibiteurs de la chaîne respiratoire
Ces inhibiteurs sont des poisons qui ont été utilisés pour identifier les intermédiaires de la chaîne respiratoire. En effet, ils ont permis d'élucider le mécanisme de fonctionnement de la chaîne respiratoire puisque leur action est particulièrement spécifique. Voici par complexe[2] :
- I - Les barbituriques, la roténone, l'amytal, la ptéricidine.
- II - Les malonates.
- III - Les antimycines A.
- IV - Le cyanure, le cobalt, les azotures, monoxyde de carbone.
- V - Le dicyclohexylcarbodiimide (DCCD), l'oligomycine, l'atractyloside.
Régulation
La régulation de la chaîne respiratoire dépend des apports en :
- NADH
- O2
- ADP+Pi
Au repos, le rapport : ![\frac {[ATP]}{[ADP+Pi]}](illustrations/0b47cc09d09bc275e82324750a69a513.png) est élevé, la chaîne respiratoire tourne par conséquent au ralenti.
est élevé, la chaîne respiratoire tourne par conséquent au ralenti.
Pendant un effort : ![\frac {[ATP]}{[ADP+Pi]}](illustrations/0b47cc09d09bc275e82324750a69a513.png) diminue, on assiste par conséquent à une augmentation de la phosphorylation oxydative (= chaîne respiratoire).
diminue, on assiste par conséquent à une augmentation de la phosphorylation oxydative (= chaîne respiratoire).
Théorie chimio-osmotique de Mitchell
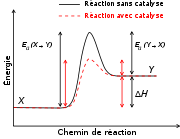
Il existe 5 ensembles de protéines et de cœnzymes impliqués dans les oxydations phosphorylantes de la chaîne respiratoire. Les 4 premiers complexes (I, II, III et IV) interviennent dans le transport des électrons et le cinquième (V) intervient dans la synthèse d'ATP (figure 2). Ces complexes diffusent de façon indépendante au sein de la membrane interne et connectés par un transporteur liposoluble mobile le cœnzyme Q (CoQ) et le cytochrome C fixé à la membrane.
- Complexe I : NADH-ubiquinone réductase ;
- Complexe II : Succinate-ubiquinone réductase ;
- Complexe III : Ubiquinone-cytochrome C réductase ;
- Complexe IV : Cytochrome oxydase ;
- Complexe V : ATP synthase.
L'expulsion d'ions H+ entraîne un gradient de pH. Les ions H+ vont revenir (dans la sens du gradient électrochimique) dans la matrice mitochondriale (ou dans le cytoplasme des bactéries) en entraînant un flux d'ions dans :
- L'ATP synthase (complexe V) entraînant la synthèse d'ATP ;
- Pour le transport de molécules contre un gradient de concentration (exemple : pompe à sodium) ;
- Pour la rotation des flagelles bacteriens.
Complexes et fonctionnement
- Complexe I : Transfert d'une paire d'électron du NADH à l'ubiquinone.
- Complexe II : Livraison d'électrons qui plus est faible énergie provenant du succinate à l'ubiquinone :
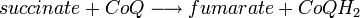 .
.
- Complexe III :
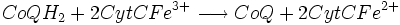
De plus, on assiste au transfert de quatre protons (H +). On peut remarquer aussi que le cytochrome c (CytC) est particulièrement conservé dans l'évolution des espèces.
- Complexe IV :
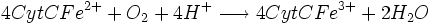
- Complexe V : Dernière étape :
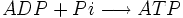 . Le flux de protons active l'ATP synthétase qui catalyse ensuite la phosphorylation de l'ADP.
. Le flux de protons active l'ATP synthétase qui catalyse ensuite la phosphorylation de l'ADP.
Les trois sous-unités β ont, à un moment donné une forme différente, en accord avec une activité fonctionnelle différente. Elles peuvent être :
- O (Open)
- L (Loose) → Faible affinité pour le substrat
- T (Tight) → Forte affinité pour le substrat
Transport des molécules d'ATP constituées
Les molécules d'ATP ainsi constituées se retrouvent dans la matrice mitochondriale où leur présence est peu intéressante. Pour passer dans le hyaloplasme, elles empruntent un anti-port, une protéine servant à faire passer de l'ATP dans le sens Matrice mitochondriale (ANT1 ou 3) → espace intermembranaire → cytosol et de l'ADP dans le sens inverse.
La différence de potentiel crée en partie par le gradient de protons induit un transport 30 fois plus rapide de l'ATP comparé à l'ADP.
Bilan total
Il dépend du nombre de protons pompés par les complexes I, III et IV, du nombre de protons utilisés pour synthétiser 3 ATP (une rotation complète de l'ATP synthase) mais aussi de l'utilisation d'énergie proton-motrice par la mitochondrie pour importer de l'ADP et du phosphate et pour exporter de l'ATP. Pour les mitochondries de levure, on estime que :
Par NADH, H +, on produit 2, 5 molécules d'ATP.
Par ubiquinone, on produit 1, 5 molécules d'ATP.
Des chaînes respiratoires spécifiques : celles des bactéries
- La chaîne respiratoire des bactéries dites «oxydase +» (Pseudomonas, Vibrio... ) est sensiblement la même que celle des mitochondries.
- La chaîne respiratoire des bactéries dites «oxydase -» (Enterobacteriaceæ... ) est plus courte : il n'y a pas le complexe IV de la chaîne respiratoire correspondant à la cytochrome oxydase.
- Occasionnellemen (respirations anaérobies chez les bactéries), l'accepteur final de la chaîne respiratoire n'est pas du dioxygène mais un composé organique comme du CO2. Voir respiration anaérobie.
Voir aussi
Notes et références
- ↑ prix Nobel de chimie à Peter Mitchell
- ↑ GARRETT R., GRISHAM C. Biochimie. Éditions De Bœck Université, Paris. 2000. ISBN 2744500208. Pages 698 et suivantes.
Liens externes
Recherche sur Google Images : |
|
"Chaîne respiratoire -" L'image ci-contre est extraite du site fr.wikivisual.com Il est possible que cette image soit réduite par rapport à l'originale. Elle est peut-être protégée par des droits d'auteur. Voir l'image en taille réelle (929 x 316 - 14 ko - )Refaire la recherche sur Google Images |
Recherche sur Amazone (livres) : |
Voir la liste des contributeurs.
La version présentée ici à été extraite depuis cette source le 06/11/2009.
Ce texte est disponible sous les termes de la licence de documentation libre GNU (GFDL).
La liste des définitions proposées en tête de page est une sélection parmi les résultats obtenus à l'aide de la commande "define:" de Google.
Cette page fait partie du projet Wikibis.


 Accueil
Accueil Recherche
Recherche Début page
Début page Contact
Contact Imprimer
Imprimer Accessibilité
Accessibilité